📅 最終更新日: 2026年2月10日 | ✍️ 著者: 法規制コンプライアンス室
健康食品・サプリメントの製造・販売には、食品衛生法・景表法・薬機法・機能性表示食品制度など複数の法規制が関わります。この記事では、天丸製薬の法規制コンプライアンス室が最新情報をもとに解説します。
💡 健康食品の法規制とは、食品衛生法・薬機法・景品表示法・健康増進法・機能性表示食品制度など、健康食品の製造・販売・広告に関わる法律・制度の総称です。違反すると行政処分や刑事罰の対象となります。
この記事の関連法規制:薬機法(医薬品医療機器等法)、景品表示法、食品衛生法、健康増進法に基づく機能性表示食品制度の実務解説。消費者庁への届出手続きと表示基準の遵守ポイントを網羅します。
機能性表示食品制度とは
⚡ この記事の要点(法規制の核心)
- 健康食品に関わる主な法規制(食品衛生法・薬機法・景表法)を整理
- 機能性表示食品の届出には科学的根拠が必須
- 天丸製薬の法規制コンプライアンス室が届出手続きをサポート
- 違反リスクを避けるための実務チェックポイントを解説
機能性表示食品とは、事業者が科学的根拠に基づき、食品の機能性(健康への効果)を消費者庁へ届け出ることで、パッケージや広告に機能性を表示できる食品制度です。2015年4月に施行され、従来の「特定保健用食品(トクホ)」に比べて、消費者庁の個別審査が不要なため、スピーディーに市場投入できる点が特徴です。
健康食品OEMを検討している事業者にとって、機能性表示食品制度の活用は差別化戦略の柱となります。本記事では、届出に必要な書類と手続きの流れを詳しく解説します。
機能性表示食品の届出に必要な書類
消費者庁への届出には、以下の書類を準備する必要があります。書類の不備があると差し戻しになるため、事前に各要件を十分確認してください。
必須書類一覧
| 書類名 | 内容・ポイント |
|---|---|
| 届出書 | 消費者庁所定の様式に従って作成。電子届出システム(Foods)を使用 |
| 安全性に関する評価資料 | 食経験の評価、または安全性試験報告書(既存情報の調査含む) |
| 機能性に関する科学的根拠資料 | システマティックレビューまたは最終製品を用いた臨床試験の論文 |
| 製品に関する資料 | 原材料・成分量・製造方法・品質管理方法を記載した書類 |
| 表示見本 | パッケージ・ラベルの最終デザイン(機能性表示、注意喚起事項を含む) |
| 健康被害情報収集体制の資料 | 健康被害が発生した場合の対応体制を示す書類 |
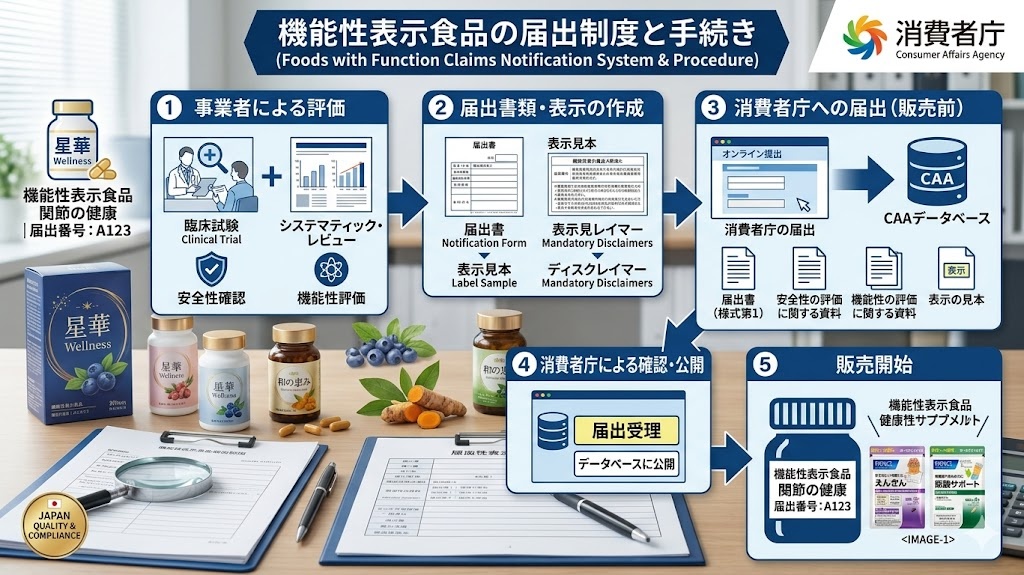
届出の流れ(ステップ別解説)
Step 1:科学的根拠の準備(最重要・最難関)
機能性表示食品の届出で最も重要かつ難しいのが、「機能性に関する科学的根拠」の準備です。根拠の示し方は2種類あります。
- システマティックレビュー(SR):関与成分に関する論文を網羅的に収集・評価し、その総合的な結果として機能性を示す方法。費用は50〜200万円程度
- 最終製品を用いた臨床試験(RCT):実際の製品を使ったランダム化比較試験。精度は高いが費用は500万円以上になることも
多くの事業者はSRを選択します。ただし、SRは専門機関(CRO:医薬品開発受託機関)への委託が一般的です。
Step 2:安全性評価の実施
機能性関与成分の安全性を評価します。評価方法は「食経験の評価」と「安全性試験」の2種類です。
- 食経験の評価:関与成分が食品として長期間、広範囲に使用されてきた場合に適用。コスト低(調査費のみ)
- 安全性試験:食経験が不十分な成分で実施。動物試験や過剰摂取試験が含まれる場合もあり、費用は高め
Step 3:製品規格・品質管理体制の整備
届出には、関与成分の含有量を製品ロット間で均一に保つための品質管理体制が必要です。OEMメーカーがGMP認証を取得していると、この要件を満たしやすくなります。具体的には以下を整備します。
- 関与成分の規格値(含有量の下限・上限)
- 規格値を確認するための試験方法
- 製造ロット管理・出荷前試験の記録体制
Step 4:パッケージ・表示の作成
機能性表示食品のパッケージには、以下の表示が義務付けられています。
- 「機能性表示食品」の文字(目立つ場所に)
- 届出番号(例:E〇〇〇)
- 機能性の表示(届出に基づく内容のみ)
- 「本品は、事業者の責任において特定の保健の目的が期待できる旨を表示するものとして、消費者庁長官に届出されたものです。ただし、特定保健用食品と異なり、消費者庁長官による個別審査を受けたものではありません。」(注意喚起文)
- 疾病の診断・治療・予防を目的としていない旨
- 摂取上の注意事項
Step 5:電子届出システム(FoSCoS)への登録・提出
2021年より、消費者庁の届出システムが「FoSCoS(Food with Functional Claims Operating System)」に移行しました。書類一式をシステムにアップロードし、電子申請します。
Step 6:審査・受理(60日間)
届出から原則60日間が審査期間です。消費者庁から問い合わせや指摘事項が届く場合があり、その都度修正・回答が必要です。届出内容に問題がなければ受理され、届出データベースに公開されます。
Step 7:販売開始
届出が受理されると(データベース公開後)、表示した機能性のある食品として販売できます。受理後も、健康被害情報の収集・報告義務が継続します。
期間と費用の目安
| 工程 | 期間目安 | 費用目安 |
|---|---|---|
| 科学的根拠準備(SR) | 3〜6ヶ月 | 50〜200万円 |
| 安全性評価 | 1〜3ヶ月 | 10〜50万円 |
| 届出書類作成・申請サポート | 1〜2ヶ月 | 20〜80万円(専門家依頼の場合) |
| 消費者庁審査 | 2ヶ月(60日) | — |
| 合計 | 最短6ヶ月〜1年以上 | 100〜400万円程度 |
届出に要する費用は製品の特性や既存エビデンスの有無によって大きく変わります。既に多くの研究論文がある成分(GABA、葉酸、イチョウ葉など)はSR作成コストを抑えやすい傾向があります。
届出を成功させるためのポイント
関与成分の選定が鍵
既に届出実績が豊富な成分(難消化性デキストリン、ルテイン、ヒアルロン酸など)を選ぶと、SR作成が比較的容易になります。届出データベースで先行事例を必ず確認しましょう。
専門家・CROへの依頼を検討する
届出書類の作成は専門的な知識が必要です。機能性表示食品の届出支援を行うCROや薬事コンサルタントに依頼することで、差し戻しリスクを下げられます。
OEMメーカーとの連携
天丸製薬では、機能性表示食品の製造実績があり、届出に必要な製造関連書類(規格書・成分分析試験報告書)の提供が可能です。届出支援機関との連携も行っており、スムーズな届出をサポートします。
まとめ
機能性表示食品の届出は、科学的根拠の準備から消費者庁への申請まで、複数のステップを経る必要があります。最短でも6ヶ月〜1年程度の期間と100万円以上の費用が見込まれますが、「機能性表示食品」として販売できる商品の信頼性・訴求力は大きなビジネス価値を生みます。
製品コンセプトと関与成分が決まったら、早めにOEMメーカーや届出支援専門家と相談することが、スムーズな届出への近道です。
機能性表示食品とトクホ(特定保健用食品)の最大の違いは何ですか?
最大の違いは審査の有無です。トクホは消費者庁の個別審査・許可が必要で費用・期間が大きく、機能性表示食品は事業者が科学的根拠を届け出るだけで消費者庁の個別審査は不要です。費用・期間ともに機能性表示食品が参入しやすいですが、トクホの方が消費者からの認知度・信頼性は高い傾向があります。