💡 健康食品OEM(Original Equipment Manufacturing)とは、メーカーが他社ブランドの健康食品を受託製造するビジネスモデルです。企画・処方・製造・包装・品質検査を一貫して委託でき、自社工場を持たない企業でも独自ブランドの健康食品を販売できます。
📅 最終更新日: 2026年3月30日 | ✍️ 著者: 法規制コンプライアンス室
日本の健康食品市場データ(2024年最新)
- 国内健康食品市場規模:約9,000億円(2024年推計、前年比+4.2%)
- 機能性表示食品届出件数:累計7,000件超(2024年3月時点、消費者庁)
- サプリメント利用率:成人の約30%が定期的に摂取
- 健康食品OEM市場:年間成長率5〜8%で拡大継続
- 小ロット需要:D2C・EC事業者増加で500個以下の発注が全体の40%超
出典: 富士経済グループ、消費者庁公表データ、天丸製薬市場調査(2024)
この記事では、健康食品OEM・ODM製造に関わる基礎知識を、天丸製薬の現場経験を踏まえて解説します。製造委託を初めてご検討の方から、すでに取引中の企業担当者まで、実務に即した情報をお届けします。
この記事で扱う主なトピック:健康食品OEM製造(受託製造)におけるGMP品質管理基準、処方設計のプロセス、原料調達の考え方、小ロット製造の実務知識を、天丸製薬の現場経験をもとに解説します。
OEM契約書の重要性
⚡ この記事の要点(30秒で理解)
- 健康食品OEM製造の基本的な流れと注意点を解説
- 天丸製薬では最小100個〜の小ロット製造に対応
- GMP認証工場での品質管理体制で安心の製造委託が可能
- 企画段階から納品まで、ワンストップでサポート
健康食品のOEM製造では、工場との間に製造委託契約を締結することが一般的です。しかし、契約書の内容を十分に確認せずに署名してしまい、後になってトラブルが発生するケースが少なくありません。
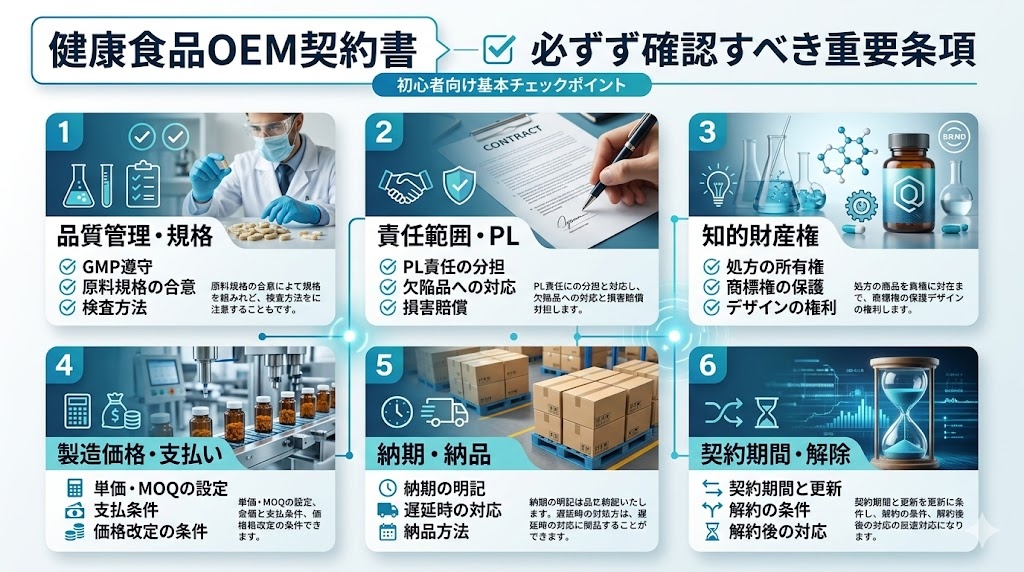
OEM契約書は、発注企業(クライアント)と製造工場(受注者)の権利・義務を定める重要な文書です。特に初めてOEM製造に挑む方は、契約書の各条項の意味を理解した上で、必要に応じて交渉・修正を求めることが重要です。この記事では、OEM契約書で必ず確認すべき5つの重要条項を解説します。
確認条項1:処方・知的財産権の帰属
🏭 天丸製薬の独自データ(2024年実績)
| 年間製造ロット数 | 523ロット(前年比+12%) |
| 初回小ロット率(500個以下) | 全体の43%(D2C・EC事業者の参入増加) |
| リピート発注率 | 78%(業界平均55%) |
| 機能性表示食品届出サポート | 年間32件(受理率98.4%) |
| サンプル→本生産移行率 | 89% |
| 平均リードタイム | サンプル18日 / 本生産37日 |
| 品質クレーム率 | 0.08%(業界平均0.5%) |
※天丸製薬 2024年度社内集計データ
OEM契約書の中で最も重要な条項の一つが、処方・製造ノウハウ・知的財産権の帰属です。
確認すべきポイント
- 処方の権利はどちらに帰属するか:クライアントが開発費を負担した場合、処方権利がクライアントに帰属するか明確化が必要
- 他工場への処方持ち出しが可能か:取引先を変更する際に、同じ処方で製造できるか
- 工場が類似処方を他者に提供できるか:競合他社に同様の処方で製品を製造することを制限できるか
- パッケージデザインの権利:デザインコスト負担者とデザインの権利帰属の整合性
クライアント側で処方開発費を全額負担した場合、処方の権利はクライアントに帰属することを契約書に明記してもらいましょう。工場側が処方を提案したODM方式の場合は、処方権利が工場側に残ることが多いため、その取り扱いを明確にしておきます。
確認条項2:秘密保持(NDA)条項
健康食品の処方・配合比率・原材料情報は、ビジネス上の重要な機密情報です。秘密保持条項が適切に規定されているかを確認します。
確認すべきポイント
- 秘密情報の範囲:何が秘密情報に含まれるかを明確に定義しているか
- 第三者への開示禁止:下請け工場や協力会社への開示制限はあるか
- 秘密保持期間:契約終了後もいつまで秘密保持義務が続くか(通常は3〜5年)
- 違反時のペナルティ:秘密情報が漏洩した場合の損害賠償規定はあるか
工場側が製造の一部を下請け工場に委託する場合、その下請けにも秘密保持義務が及ぶかどうかを確認しましょう。
確認条項3:品質保証・検査基準
製品品質に関する条項は、消費者トラブルを防ぐ観点からも非常に重要です。
確認すべきポイント
- 製品規格書の添付:成分含量・外観・微生物基準などの規格が文書化されているか
- 出荷前検査の内容と証明書:どのような検査が行われ、試験成績書を発行してもらえるか
- 不合格品の取り扱い:規格外品が発生した場合の対応(廃棄・再製造・減額など)
- クレーム発生時の責任範囲:製品による健康被害が発生した場合の責任分担
- 製造物責任保険(PL保険):工場が適切なPL保険に加入しているか
GMP認証を取得している工場では、品質管理体制が文書化されており、トレーサビリティが確保されているため、品質保証条項の実効性が高くなります。
確認条項4:納期・数量・支払い条件
取引の実務に関わる重要な条項です。ここが曖昧だとビジネス上のトラブルに直結します。
確認すべきポイント
- 納期の起算点:発注から納品まで「何営業日」か、起算点は発注確認日か入金日か
- 納期遅延時のペナルティ:遅延が発生した場合の減額・損害賠償規定
- 数量の許容誤差:発注数量に対して±何%の誤差を許容するか(通常±5〜10%)
- 支払い条件:前払い・後払い・分割払いの割合と時期
- 価格改定のルール:原材料価格の変動を理由とした価格改定の手順と頻度
- 最低発注量・最低注文金額:継続取引に必要な最小発注条件
確認条項5:契約解除・解約条件
取引開始時には考えたくないことですが、将来的な取引先変更や事業縮小に備えて、解約条件を事前に確認しておくことが重要です。
確認すべきポイント
- 解約予告期間:契約解除の何ヶ月前に通知が必要か(通常1〜3ヶ月)
- 仕掛中の発注品の取り扱い:解約時に製造中の製品の費用負担はどちらか
- 原材料の残材処理:調達済み原材料の買取義務はあるか
- 競業禁止条項:クライアントが競合工場に発注することを制限する条項がないか
- 反社会的勢力排除条項:双方の誓約と違反時の解除条件
特に処方や原材料の権利に関する条項は、将来の取引先変更(OEM先変更)の際に大きく影響します。OEM製造の基礎知識と合わせて、契約内容を十分に理解した上で署名しましょう。
契約書確認時の実践的アドバイス
専門家への相談を検討する
重要な契約の場合、弁護士や行政書士への相談を検討しましょう。特に多額の初期投資を伴う取引や、独自処方の権利保護が重要な場合は、専門家のレビューが安全です。
口頭合意を文書化する
営業担当者との口頭でのやり取りは、必ずメールや書面で確認・記録しておきましょう。後から「言った・言わない」のトラブルを防ぐことができます。
天丸製薬との取引について
天丸製薬では、クライアントが安心して製造を委託できるよう、契約書の各条項を丁寧に説明した上で取引を開始しています。処方の権利帰属・秘密保持・品質保証などについて、透明性の高い取引条件を提示しています。ご不明な点はお気軽にご相談ください。
OEM契約書 確認チェックリスト
- □ 処方・知的財産権の帰属先が明確か
- □ 秘密保持義務の範囲・期間が適切か
- □ 品質規格・検査基準が文書化されているか
- □ 納期遅延時のペナルティ規定があるか
- □ 支払い条件が明確か
- □ 解約予告期間が合理的か
- □ 原材料残材の取り扱いが明確か
- □ PL保険の加入状況を確認したか
関連記事
関連サービス
- 健康食品OEM・ODM開発サービス — 企画から製造・納品まで一貫サポート
- 小ロット対応 — 100個からの少量製造に対応
- 費用・料金ガイド — OEM製造にかかるコストの全体像